Le stress oxydant est une des conséquences de la vie aérobie qui entraîne inévitablement la formation d’espèces réactives de l’oxygène. Les organismes vivants ont donc mis en place des systèmes permettant de détecter ce stress oxydant afin d’activer des mécanismes de protection.
En collaboration avec l'iRTSV et l'IBS, nous avons mis en évidence un mécanisme radicalement nouveau de détection par une protéine du stress oxydant induit par l’eau oxygénée (H
2O
2). Face à de tels agents, les protéines s’oxydent généralement au niveau d’un acide aminé particulier, la cystéine. Dans le cas de la protéine PerR, il a été montré que H
2O
2 oxyde un autre acide aminé, l’histidine. L’oxydation de cet acide aminé confère à la protéine de nouvelles propriétés et la diminution de son affinité pour l’ADN, lui permet de réguler de nombreux gènes en réponse au stress oxydant. L’identification des produits de réaction a été réalisée sur l’équipement HPLC-MS/MS de notre laboratoire (chromatographe en phase liquide couplée à un spectromètre de masse en mode tandem).
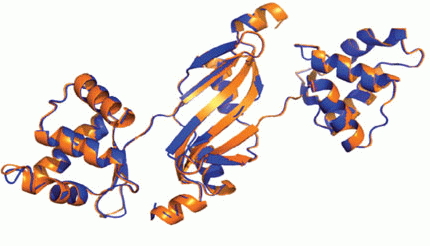
Structure cristalline de la protéine oxydée PerR-Zn-ox.