Une récente approche visant à la destruction de cellules cancéreuses a été proposée, basée sur le déclenchement de la mort spontanée des cellules cancéreuses, grâce à la vibration mécanique de nanoparticules magnétiques anisotropes attachées aux membranes cellulaires, à basse fréquence (20 Hz) et en faibles champs magnétiques (quelques mT). L’induction de l’apoptose des cellules cancéreuses a été démontrée à partir de particules de NiFe en vortex, par des mesures statistiques de cytométrie en flux et l’étude de l’activation des caspases.
Les micro/nanoparticules magnétiques sont d’un grand intérêt pour les applications biomédicales, car elles permettent d’exercer des forces à distance sur les espèces biologiques. Nous avons démontré sur des cellules du carcinome rénal humain, que cela peut être utilisé pour tuer des cellules cancéreuses, travaux récemment publiés dans
Nanoscale. Sachant qu’au moins 20% des êtres humains risquent d’être confrontés à un cancer au moins une fois dans leur vie d’ici 2020, cette étude ouvre la perspective d’une nouvelle approche thérapeutique pour le cancer, avec des effets secondaires réduits. Cette approche biomédicale est très différente de l’hyperthermie abondamment étudiée, car elle repose sur un effet mécanique à basse fréquence (~20 Hz), et non pas sur un chauffage local des cellules par les champs AC de hautes fréquences utilisés en hyperthermie (100 kHz, 10 mT). Les particules ont été préparées par une approche « top-down ». Différents types de particules ont été préparés et testés avec le but d’éviter leur agglomération en solution, et celui d’exercer de forts forces et couples lorsqu’elles sont attachées aux membranes cellulaires. Les disques de NiFe en configuration de vortex magnétiques ont été sélectionnés, et recouverts de couches d’or pour permettre leur fonctionnalisation biochimique (Figure a). Ces particules en vortex magnétiques ont ensuite été reliées aux membranes des cellules du carcinome rénal humain, par la reconnaissance anticorps-antigène. Pour cela, la lignée cellulaire cancéreuse a été transfectée pour exprimer un antigène spécifique de surface, appelé « anhydrase carbonique 9 humain » (hAC9), biomarqueur de l’hypoxie tumorale. Le lien entre particule et cellule cancéreuse a été obtenu à l’aide d’un anticorps anti-hAC9 de lapin. Après le traitement basé sur l’application d’un champ AC de basse fréquence, une diminution de ~70% de cellules vivantes a été observée 6 heures après le stimulus magnéto-mécanique (Figure c). L’induction de l’apoptose des cellules cancéreuses a ensuite été démontrée par cytométrie en flux (Figure d). En outre, une augmentation significative, après traitement, de l’activation des caspases-3/7, composant clé de la machinerie apoptotique, a été observée au microscope. Cette étude sera poursuivie en collaboration avec Clinatec par des essais
in vivo, et l’espoir, à plus long terme de développer un réel traitement du cancer.
Cette étude multidisciplinaire est le résultat d’une collaboration entre Spintec, SPrAM/CREAB, SCIB/LAN, THEREX/CHU, SP2M/NM, et l’utilisation de la salle blanche PTA.
Remerciements : Travail partiellement financé par l’Agence Nationale de la Recherche via le projet P2N Nano-Shark ANR-11-NANO-001, et par la Région Rhône-Alpes via CIBLE 2012.
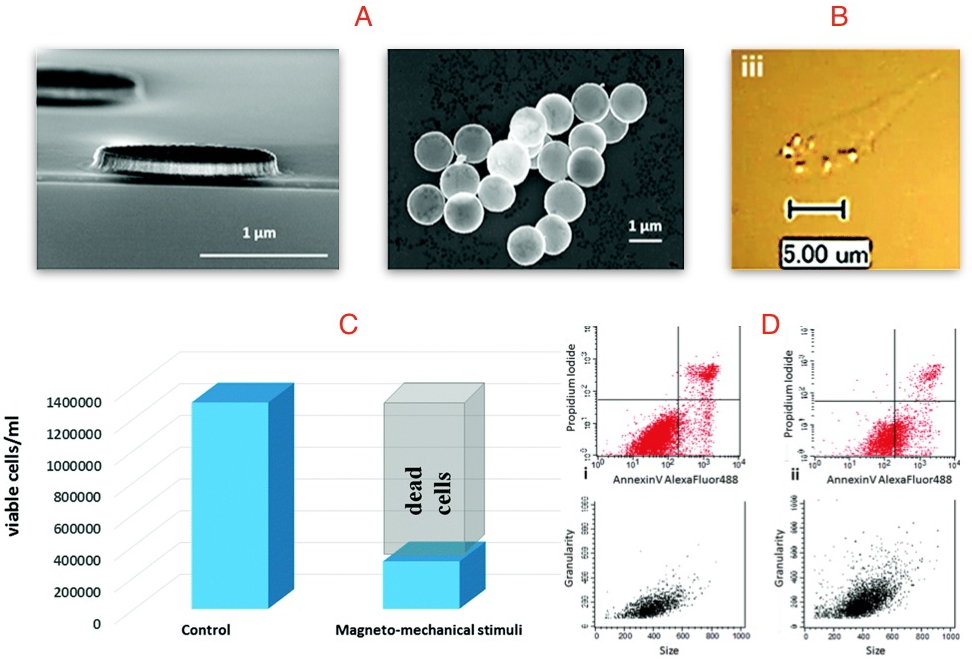
a) Particules de NiFe en configuration de vortex magnétiques ∅1µm.
b) Cellule cancéreuse à laquelle six particules fonctionnalisées sont fixées.
c) Proportion de cellules restant en vie, coloration au bleu trépan.
d) Analyse par cytométrie de flux de l'annexine V et coloration à l'iodure de propidium.